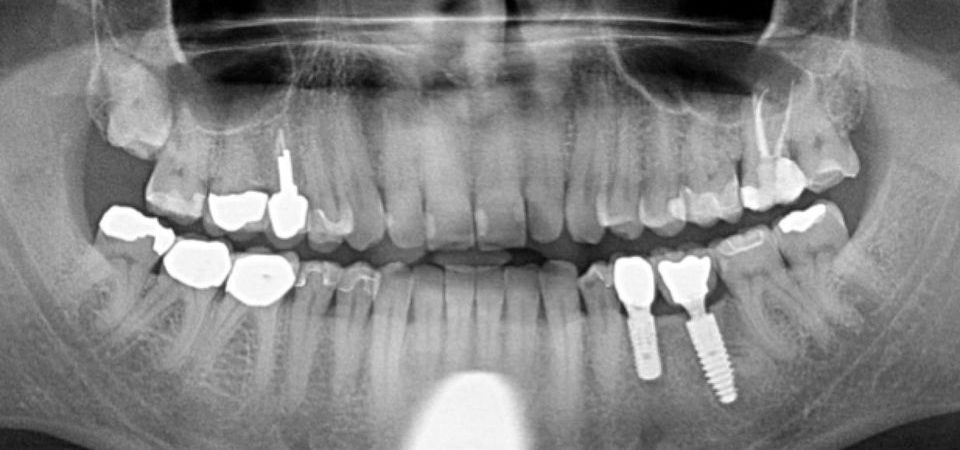
Und warum ist Zirkonium (als Oxid) als schweres Homologes von Titan deutlich geeigneter als Titan (als Metall)?
Kieferherd vs. Zahnherd
Beim Absterben des Zahnnervs pasieren mehrere Dinge gleichzeitig.
So werden etwa die Verbindungen zunehmend gekappt, und zwar zwischen lebendigem Gewebe IM Zahn und lebendigem Gewebe in Pulpamaterial und Zahnkiefer, also lokalem Knochengewebe.
Die Pulpa wird mit der Invasion von Gärungs- und Fäulnisbakterien sowie deren toxischen Stoffwechselprodukten nicht mehr fertig und wird bakteriell zersetzt: mit allen Konsequenzen des anaeroben Stoffwechsels, die ihrerseits wieder Metalle ansammeln. Denn: die Knochensubstanz ist weiter lebendig, ganz im Gegensatz zum Zahnmaterial (!).
Bei toten Zähnen muss also deutlich unterschieden werden zwischen Kieferherden (oft ‚NICO’s‘ genannt) und Zahnherden.
Kieferherde entstehen im Zuge lokaler Entzündungen, die mit Organen und Meridiansystemen verbunden sind (wie auch im ersten Teil beschrieben).
Kiefermaterial ist sehr anfällig gegenüber dem Mundmikrobiom und knochenrelevanten Mikronährstoffmängeln. Aber es ist auch sehr anfällig gegenüber oxidativem Stress – verursacht durch zB. Telefonieren. Der Einfluss in Breite und Tiefe wird (buchstäblich) vielfach deutlich unterschätzt und kann zum biochemisch bedingten Abbau von Knochenmaterial, Aktivität von Osteoklasten und Parathormon, Makrophagen und damit zur Eiterbildung und Entzündungsanheizung beitragen.
Die Haltbarkeit von Zahnmaterial im ‚toten‘ Zustand ist unterschiedlich – wird etwa definiert vom Kollagenzustand und Mineralisierungsgrad zum Zeitpunkt des Absterbens und damit ‚Verlegens‘ der Dentinkanäle. Eine zeitnah durchgeführte Depotphorese kann desinfizieren und den Zahn – obwohl tot – recht lange entzündungsfrei halten.
Eine Wurzelspitzenresektion am toten Zahn zerstört natürlich alle feinen Kanäle an der Zahnspitze – dort befinden sich erfahrungsgemäß die meisten Nerven und Kanäle, da die biochemische Kontaktoberfläche in dieser Region am größten ist.
Eine Spitzenresektion oder auch ein zu langes Warten nach Absterben des Zahns hat mit einiger Wahrscheinlichkeit eine Herdproblematik zur Folge, die ein Abwägen auf Zeit und schlussendlich ein Entfernen des Entzündungsgeschehens erfordert. Lokale Verkalkungen könnten auch zu Einschlussverbindungen von Toxinen führen; dies nachzuweisen ist allerdings schwierig.
Allerdings sind Einflüsse der Nachbar’Kieferregion‘ hier überlappend – mit unklaren Auswirkungen.
Das ‚Verlegen‘, also der Verschluss der überaus feinen Dentinkanälchen schließt Bakterien, Makrophagen, aber auch Toxine mehr oder weniger fest in den Zahn ein. Möglich ist also eine lokale Ansammlung von Enztündungsherden, die die Zahnsubstanz chemisch von innen schädigen. Auch wird die feine ’schwammartige‘ Struktur des vorher gesunden Materials langsam verstopft und vergröbert – vielleicht auch verkalkt. Man könnte auch sagen: der gleichmäßig feinverteilte Austausch reduziert sich auf die noch ‚offenen‘ Poren.
Diese spielen die Schlüsselrolle für ein späteres Geschehen und bestimmen Art; Schwere und Intensität der ‚Herdaktivität‘ – bezogen auf den toten Zahn!
Es ist also denkbar, dass wenige Kavitäten erhalten bleiben für einen Austausch mit der Mundflora: eine permanente ‚Dauerentzündung‘ ist vorprogrammiert.
Bedeutung für den Zeitpunkt des Zahnersatzes
Das alles hat individuelle Auswirkungen auf den Zeitpunkt und den Umfang von Zahnmaterialersatz.
Auch eine Elektrosmogfreiheit sowie ein Heilen des Materials spielen eine sehr sehr große Rolle.
Gegebenenfalls mag eine Sanierung von Mundmikrobiom erforderlich sein (Zahnreinigung, Ultraschall, Ozon oä.).
Und: es gibt große Unterschiede in Materialien, die aus Kunststoff bestehen und welchen mit mehr oder weniger Keramikanteil.
Titanmaterialien
Dazu wird es in Kürze auch einen weiteren podcast geben (allgemeines Thema: Knochen, Osteoporose und Co.), weil das buchstäblich ‚in aller Munde‘ ist – um einen Buchtitel zu bemühen.
Die Sicht der Chemie
Eine weitere Wechselwirkung ist die mit Fluorid. Das ist leider umstritten, hat aber gleichwohl eine sehr große Wechselwirkung mit natürlichem Zahnmaterial – eben dem Calciummonofluorphosphat – aber auch mit Silizium, das etwa fähig ist, Fluorid zu binden. Im Ca5[F(PO4)3] kann das Fluorid dabei durch Hydroxid-Ionen ersetzt werden und das Material dabei an Härte verlieren. Die Frage ist, ob eine Fluoridierung die Zähne härter und widerstandsfähiger macht, oder ob dabei die Zähne zwar hart, aber auch brüchiger werden (was im Übrigen auch für die Kieferknochen gelten kann). Die komplexe Zusammensetzung des Apatits in der Natur bildet im Zahnschmelz ein Gegenstück des menschlichen Körpers. Hier darf auch Kieselsäure als Regulator seine Rolle finden – und es sind noch viele Dinge ungeklärt.
Ein weiteres kompliziertes Thema wäre die Rolle des silikathaltigen Glasionomerzementes und dessen Haftungseigenschaften an natürliches Zahnmaterial…
Literatur (neben den in Teil 1 genannten):
1. Lechner, Johann & Noumbissi, Sammy & von Baehr, Volker. (2018). Titanium implants and silent inflammation in jawbone—a critical interplay of dissolved titanium particles and cytokines TNF-α and RANTES/CCL5 on overall health?. EPMA Journal. 9. 10.1007/s13167-018-0138-6.
2. Dominik Nischwitz: In aller Munde. Unsere Zähne und ihre Bedeutung für die Gesundheit des ganzen Körpers. Mosaik Verlag,2019. ISBN: 978-3-442-39343-5
3. Podcast zum Knochenstoffwechsel, Osteoporoseprävention und Zusammenhängen