Aufgrund vieler Rückmeldungen, Erfahrungsberichten und dem Studium entsprechender Literatur ist es Zeit für eine Bestandsaufnahme, was die Nierengesundheit angeht.
Das ist auch deshalb bedeutsam, weil die gesamte (traditionelle) Chinesische Medizin darauf ausgerichtet ist, die Nierengesundheit (Nieren-Qi) zu stärken und auszugleichen.
Hier hat sich Silizium als echtes Adaptogen erwiesen.
Warum?
Zunächst ist es wichtig zu betonen, dass es ein Gleichgewicht zwischen Kieselsäuren und Siliziumdioxid gibt, das an die Anwesenheit von Wasser und mikrobielle Aktivitäten gebunden ist. Das hat unter anderem auch Guy E. Abraham beschrieben (2, in neuerer Zeit); eigentlich erstaunlich, denn Abraham war eher bekannt für seine Forschungen zum Thema Jod (eine weitere historische Verbindung findet sich in dem Buch von Prof. A. Kühn: die Kieselsäure (1926). Weitere Literatur findet sich unten bzw. in den dort zitierten Studienübersichten).
Dieses Gleichgewicht reguliert den Wasserhaushalt im Körper entscheidend mit und bestimmt die renale Exkretion oder auch die fäkale Exkretion, also ob die Kieselsäure über den Darm oder die Nieren ausgeschieden wird.
Dazu könnte ich Berge an Literatur anführen, was allerdings wenig Sinn macht. Denn jeder wird schon einmal erfahren haben, wie es ist, ganz dringend Pipi zu müssen, wenn er einen Brennnesseltee, einen Bambustee oder Ackerschachtelhalmtee getrunken hat; gleiches gilt für kolloidale Kieselsäureprodukte – hier vor allem in wässriger Form.
Darauf beruhen weitere erfahrungsmedizinische Analysen und Provokationsstudien zum ‚Ausschwemmen‘ von Toxinen, was tatsächlich einen ernsten Hintergrund hat.
Es ist also wichtig festzuhalten, dass diese Provokation den Nieren ‚Arbeit‘ gibt – in Form des ADH und der Aufkonzentrierung des Primärharns.
Dieser Prozess findet in den Nieren statt, hier vor allem den Nierenglomeruli.
ZU wenig trinken ist vor allem für ältere Menschen fatal; allerdings tun sich hier auch subtile Fragen auf: was ist eine gute Dosis? Kann ich meine Nieren damit ‚überladen‘?
Schwemme ich mit Kieselsäure zu viele Mineralien aus?
Wo liegen die Grenzen zwischen Wassertransport und Wasserbindung? Oder – anders gefragt: kann ich mit einer Kieselsäure auch Wasser in den Körper einlagern?
Und: wird auch nicht einiges fäkal ausgeschieden?
Das sind allesamt sehr komplexe Fragen, die nicht nur die Kieselsäurewirkung berühren, sondern auch die Cofaktoren. Und das kann tatsächlich beliebig komplex werden, weil nicht nur die Anzahl der Cofaktoren und ihre Synergie komplex sind, sondern auch deren individuelle Dosierung.
Beispielsweise wurde in den letzten Jahren gezeigt, dass eine Therapie von Silizium, Vitamin D3 und Ca einer Therapie von Vitamin D3 und Ca signifikant überlegen ist (allerdings waren die Studiendesigns und -zeiträume wie so oft viel zu kurz, 3). Dies alleine ist bedeutsam vor dem Hintergrund, dass immer noch nicht in der Praxis angekommen zu sein scheint, dass wir nicht 800 IE D3 täglich brauchen, sondern eher 7000-8000 IE (bezogen auf das, was im Körper ankommen soll, und NICHT was wir substituieren!).
Silizium als echter Regulator
Insgesamt tut sich also hier ein komplexes ‚Waagebalkenbild‘ auf, das der Kieselsäure die Bezeichnung ‚Feuerwehr‘ eingetragen hat.
Kieselsäure ist demnach nicht nur ein Wassertransporter, sondern auch ein Transporter für Calcium, für Mineralien und Spurenelemente, aber auch für Proteine (60%) und Fette (30%). Die frühen Untersuchungen von Hugo Schulz sind im wesentlichen bestätigt worden durch die Arbeiten von Carlisle, Birchall, Iler, Brinker und Scherer, Jugdaohsingh, Exley, Canham und anderen.
Die Grenze zwischen Transport und Bindung liegt bei etwa 120-150 ppm, vielleicht auch noch etwas darüber. Aber warum so unscharf?
Das liegt unter anderem an der biochemischen Individualität – und vor allem an der Nierenleistung, die ja hier vor allem Thema ist.
Das hat zu erheblichen Missverständnissen geführt wie etwa ‚ich habe noch nie Silizium supplementiert, habe aber einen zu hohen Wert. Wie kann das sein?‘
Dazu ist zu sagen: Auch eine Hyperkaliämie ist Zeichen einer schlechten Nierenfunktion, denn: ein ZU viel an Kalium im Blut bedeutet gerade bei schweren und konsumierenden Erkrankungen auch ein ZU wenig in den Zellen und eine Unterversorgung der Extrazellularmatrix, in der Kieselsäure eine buchstäblich grundlegende (Spül)Funktion erfüllt.
An anderer Stelle hatte ich schon auf die Regulation des Blutdrucks hingewiesen und die Rolle von Silizium im Transport von Wasser und Mineralien bzgl. Aquaporine (6), s. auch https://bruno-kugel.de/silizium-und-bluthochdruck-eine-epidemie/.
Ein weiterer Grund ist das komplexe Gleichgewicht oligomerer Kieselsäuren, die sowohl pH-abhängig als auch von der Anwesenheit von Mineralien abhängig ist. Das ist schon recht früh – etwa von Iler – beschrieben worden und später auch anhand von Kristallstrukturanalysen bestätigt worden; damit wurde bewiesen, dass mehrere Kieselsäuren nebeneinander existieren können und so eine regulierende Funktion ausüben.
Das ist im weiteren dann auch ein Problem der Referenzierung, denn: wie will man das auf eine Gehalt beziehen, wenn man keine einzelne Substanz hat, auf die man sich beziehen kann?
150 ppm Orthokieselsäure ist nicht gleich 150 ppm Dikieselsäure – oder Trikieselsäure.
Das schein ein grundlegendes Thema gerade beim Silizium zu sein.
Ein mögliches Erklärungsmodell
Es scheint aber so zu sein, dass oberhalb von 200 ppm der Körper reguliert und Wasser sowie Kieselsäure vermehrt ausscheidet. Und das ist auch gut so, denn das befeuert den Stoffwechsel, die Mineralienausscheidung (mit der auch Toxine und endogene Stoffwechselprodukte ausgeschieden werden), den Wasserhaushalt, die Befeuchtung der Nierentubuli, das ‚Training‘ der Enzymkaskaden – hier vor allem des RAAS-Systems und damit der Blutdruckregulation, die ja bekanntlich über die Blutmenge, also die Natrium’retention‘ in den Nieren erfolgt.
Das wiederum hängt mit der Eigenschaft von Natrium zusammen, mehr Wasser anzuziehen als das größere Kalium-Ion. Vielleicht auch deshalb ist die Evolution so gelaufen und Kalium ist das zweithäufigste Mineral in unserem Körper.
Und: die Natrium-Kalium-Pumpen sind Aquaporine, also Ionenpumpen, die unter ATP-Verbrauch die Ionengradienten aufrechterhalten. Wenig Energie à wenig ATP à wenig Kraft. Nicht nur für die Muskulatur, sondern auch wenig ‚Spannung‘ und ‚Potential‘.
Also wesentlich mehr als 200 ppm im Blut wird man unter normalen Umständen nicht finden.
Wenn, ist das als zunehmend pathologisches Zeichen zu sehen, ähnlich wie bei einer Hyperkaliämie.
Der Körper wird versuchen, sich dieses Überschusses zu entledigen: durch forcierte Diurese.
Diese kann passiv erfolgen, aber auch aktiv erfolgen.
Übrigens: kleine Moleküle werden eher renal ausgeschieden, während größere eher über den Darm ausgeschieden werden.
Ein sehr grobes Modell, was aber in der Biochemie und Physiologie, Pharmakologie und Toxikologie ein allgemein akzeprtierter Fakt ist.
Auch hier spielt wieder das Phänomen ‚Alterung‘ mit: bei ‚gealterten‘ Strukturen kann weniger Wasser festgehalten werden und wird schneller ausgeschieden, ohne relevante Organbereiche zu ’sehen‘.
In der Praxis ist deshalb oftmals zu beobachten, dass unter Siliziumsubstitution vermehrter Durst zu beobachten ist; gleichzeitig ist der Bedarf an Mineralien möglicherweise auch erhöht.
Das scheint nicht immer der Fall zu sein und ist ein dosisabhängiger Befund, der sich im Verlauf einer kontinuierlichen Substitution auch einregelt.
Bei verminderter Nierenleistung ist Vorsicht geboten, was die Kapazität und Geschwindigkeit der Ausscheidung angeht: bekanntlich regulieren Schilddrüsenhormone und Wachstumshormon die Aufnahme von Silizium (Holzer & Holzer, 2008 und dort zitierte Literatur); das ist einer der Gründe, warum wir eine derart weit verbreiteten subtilen Siliziummangel haben.
Manche Anwender berichten auch – gerade bei mineralienhaltigen Produkten – von Schwindel bis hin zu Übelkeit. Gerade dann, wenn sie zu wenig getrunken haben und eine größere Dosis auf einmal genommen haben.
Das kann dann auch die Nieren temporär belasten; hier kommt es auf das Produkt und die zeitnahe Flüssigkeitszufuhr an, wie sich das im weiteren Verlauf auswirkt.
Ich beschreibe das auch gerne mit dem Begriff Reizmittel‘, was schon früher von A. Kühn geprägt wurde, allerdings unter anderer Anwendungsform.
Die Reaktion auf diesen Reiz ist entscheidend; allerdings bestimmt auch die Dosis und die Art der Applikation (Si + X) die Wirkung.
Eine mehrfach beschriebene Wirkung (auch in der FB-gruppe zum Erfahrungsaustausch und der Erforschung von Wirkungen von Silizium als ‚Baustein des Lebens‘) ist die einer deutlichen Wirkung anfangs und dann einer Eingewöhnung mit nahezu ausschließlich positiven Wirkungen (nahezu, weil es eben manchmal nix tut. Negativwirkungen sind allerdings bei Einhaltung der empfohlenen Dosierungen nicht beschrieben worden).
Insbesondere auf einen Aspekt möchte ich noch eingehen.
So wurde berichtet, dass bei ‚schaumigem Urin‘ die ‚Schaumbildung‘ unter Si-substitution weniger wurde bis aufhörte.
Ein bemerkenswerter Befund in mehrfacher Hinsicht.
Zum einen ist es so, dass Silizium sich an Proteine und hier besonders Lipoproteine bindet (7) und diese auch zu regulieren vermag. Hier zeigt sich auch der Zusammenhang mit LDL, Cholesterin und einer Hyperlipoproteinämie, also einem zu viel an schlechten Blutfetten und zu viel Protein im Blut (weil dem Körper die Kraft fehlt, das entweder auszuscheiden oder zu verstoffwechseln).
Zum anderen ist es so, dass gerade im Zuge einer Siliziumzufuhr mehr Wasser im Körper zirkuliert und demzufolge der Körper besser Toxine ausschwemmen kann. Dazu können auch physiologisch vorkommende, aber in ihrer Menge überbordende Proteine und Peptide gehören.
dieser Prozess funktioniert langsam, aber kontinuierlich.
Ein weiterer Aspekt, der sehr gut als Erklärungsmodell dienen kann:
Siliziumdioxid und Kieselsäurepräparate werden als ‚anti-foaming agents‘ (in wechselnder Komposition, auch patentiert) eingesetzt. Die Funktion in unserem Körper als ‚Anti-schaum-mittel‘ ist daher mehr als gerechtfertigt.
Der genaue Wirkmechanismus ist nicht ganz genau verstanden, hängt aber gleichwohl von der inneren Oberfläche der Teilchen, ihrer Natur (polar/unpolar, ionisch oder nicht-ionisch) in passgenauer Wechselwirkung mit entsprechenden Lipoproteinen im Körper zusammen.
Hier kommt es tatsächlich auf molekulare Details UND auf Teilchengrößen an.
Wie viel Kieselsäure ist für die Nieren wirklich ‚gut‘?
Eine sehr wichtige Frage, die einer biochemischen Individualität unterliegt. Kieselsäurehaltige Mineralwässer alleine reichen hier nicht aus; diese haben übrigens ca. 120-150 ppm Kieselsäure mit einer sich schnell abspielenden ‚Kinetik‘: nach geschätzt 4-5 Stunden ist das meiste bereits wieder ausgeschieden; das zeigen Provokationsstudien (zb. 2a-c).
Im Zuge einer Substitution ist zwingend auf ausreichend Bewegung zu achten, damit das piezoelektrische und System und das elektrophysiologische System Mensch die Verteilung gewährleisten kann.
Hier ist die Empfehlung der EFSA ausnahmsweise tatsächlich sinnvoll: Mengen bis 350 mg Kieselsäure täglich in kolloidaler Form sollten nicht überschritten werden (eigene Beobachtung, aber: KEIN IMPERATIV!!!).
Gemäß dem individuellen Bedarf kann die jeweils benötigte Kombination unterschiedlich ausfallen.
Es kann aber als gesichert gelten, dass eine Überladung des nichtlinear-selbstregulierenden Systems Mensch mit Kieselsäure aus natürlichen Quellen nahezu ausgeschlossen ist.
WENN eine Überladung stattfindet, ist diese fokal bedingt und an Stellen, wo eine kolloidale Alterung stattgefunden hat. Dies ist im allgemeinen für das System Nieren nach derzeitigem Stand ausgeschlossen, es sei denn, es wird VIEL zu wenig getrunken ODER es liegen schwerwiegende Erkrankungen der Nieren vor, die eine Aufkonzentration des Primärurins vermindern bis verhindern – in die ein oder andere Richtung (Anurie oder Polyurie bzw. Diabetes insipidus, um zwei diametrale Gegensätze zu nennen).
Apropos Diabetes: hier könnte Silizium auch dazu beitragen, den Zuckerstoffwechsel bei Diabetes mellitus Typ 2 auszugleichen (8).
Allgemein ist es nach Praxiserfahrung so, dass vor allem die Regulation von Ca:Mg, Na:K und damit auch von Phosphat im Blut über Kieselsäure gesteuert wird. Was kein wirklich überraschender Effekt ist, wenn man sich die Literatur genauer anschaut.
Zusätzlich scheint es so zu sein, dass hier – bei ausreichender Trinkmenge – auch pathogenreduzierende Eigenschaften der Kieselsäure wichtiger werden; entweder sie werden einfach ausgeschwemmt oder sie können nicht mehr an das Nierenepithel binden und Schäden verursachen (weil ganz einfach gesagt die Schleimhaut gestärkt wird). Das kann mechanisch, abe5r auch biochemisch geschehen (über Fibroblastenaktivierung, verbesserte Wasserspeicherung des Gewebes, endokrine Steuerungsmechanismen und neurologische Prozesse).
Bei verminderter Nierenleistung – hier vor allem weniger als 50-60 ml/min – muss die Substitution ggf. angepasst werden.
Allerdings wirft das alles viele weitere Fragen auf, die den Kieselsäurestoffwechsel in den Nieren erforschen lassen wollen.
Das sind übrigens nur exemplarische Erklärungsmodelle; den kompletten Stoffwechsel hier erfassen zu wollen – inklusive zb. Kalium oder Vitamin C – ist illusorisch und wurde meines Wissens so noch nie unter dem Aspekt von Kieselsäure betrachtet.
Gleichwohl erscheint es höchst notwendig – angesichts der vielen biochemischen Wirkungen von kolloidaler Kieselsäure – das zu ändern und zumindest Thesen aufzustellen und diese durch entsprechende Studien zu verifizieren oder zu falsifizieren.
Das ist echte Wissenschaft und wird das Verständnis der so wichtigen, aber in Vergessenheit geratenen und für die biochemische Kommunikation so wichtigen Kieselsäure voranbringen.
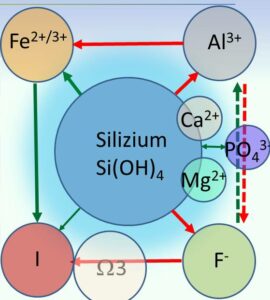
EIN immer häufiger kursierendes Bild ist das folgende.
Es zeigt, dass Kieselsäure direkt mit Phosphat wechselwirkt und dass die Variation der Ca/Mg- Verhältnisse hier eine wesentliche Rolle spielen.
Dasselbe gilt für die Variation der Na/K-Verhältnisse.
Grüne Pfeile: beeinflusst sioch positiv/wirkt synergetisch
Rote Pfeile: beeinflusst sich negativ/wirkt antagonistisch
Diese Grafik ist keinesfalls komplett!
P.S.: Verwendung unter Nennung des Autors wäre nett.
Das ist ein Experiment. Mal ehen wo das landet.
|
Literatur
- Guy Abraham, The Importance of bioactive silicates in human health https://www.optimox.com/content/Iodine%20Research%20Resources/bioactive-silicates.pdf
- a) J.W. Dobbie, M.J.B. Smith; Urinary and serum silicon in normal and uraemic individuals; Ciba Foundation, Symposium 121: Silicon biochemistry (1986), 194ff.
b) Magnusson C, Jugdaohsingh R, Hulthen L, Westerlund A, Powell JJ, Ransjö M. Urinary Excretion of Silicon in Men, Non-pregnant Women, and Pregnant Women: a Cross-sectional Study. Biol Trace Elem Res. 2020 Apr;194(2):321-327. doi: 10.1007/s12011-019-01785-5. Epub 2019 Jun 29. PMID: 31254248; PMCID: PMC7015958.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7015958/
c) Diss. Marian Waterstradt (2019; Resorption von Equisestum arvense-Zubereitungen – eine randomisierte aktiv kontrollierte Pilotstudie
- Rondanelli M, Faliva MA, Peroni G, Gasparri C, Perna S, Riva A, Petrangolini G, Tartara A. Silicon: A neglected micronutrient essential for bone health. Exp Biol Med (Maywood). 2021 Jul;246(13):1500-1511. doi: 10.1177/1535370221997072. Epub 2021 Mar 9. PMID: 33715532; PMCID: PMC8283247.
- Veugelers PJ, Ekwaru JP. A statistical error in the estimation of the recommended dietary allowance for vitamin D. Nutrients. 2014 Oct 20;6(10):4472-5. doi: 10.3390/nu6104472. PMID: 25333201; PMCID: PMC4210929.
- https://pubmed.ncbi.nlm.nih.gov/?term=silicic+acid+renal+failure&filter=pubt.clinicaltrial (abgerufen am 8. August 2024)
- a) Azad AK, Raihan T, Ahmed J, Hakim A, Emon TH and Chowdhury PA (2021). Human Aquaporins: Functional Diversity and Potential Roles in Infectious and Non-infectious Diseases. Front. Genet. 12:654865. doi: 10.3389/fgene.2021.654865.https://www.frontiersin.org/journals/genetics/articles/10.3389/fgene.2021.654865/full
b) Garneau AP, Carpentier GA, Marcoux AA, Frenette-Cotton R, Simard CF, Rémus-Borel W, Caron L, Jacob-Wagner M, Noël M, Powell JJ, Bélanger R, Côté F, Isenring P. Aquaporins Mediate Silicon Transport in Humans. PLoS One. 2015 Aug 27;10(8):e0136149. doi: 10.1371/journal.pone.0136149. PMID: 26313002; PMCID: PMC4551902.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4551902/
- : A.A. Chuiko, A.A. Pentyuk, and V.K. Pogorelyi, Enterosorbent Silics: Properties and Clinical Application in: H. Bergna, Colloidal Silica: Fundamentals and Applications, 177-186; hier besonders Tabellenübersichten.
- Hernández-Martín M, Bocanegra A, Redondo-Castillejo R, Macho-González A, Sánchez-Muniz FJ, Benedí J, Bastida S, García-Fernández RA, Garcimartín A, López-Oliva ME. Could Duodenal Molecular Mechanisms be Involved in the Hypocholesterolemic Effect of Silicon Used as Functional Ingredient in Late-Stage Type 2 Diabetes Mellitus? Mol Nutr Food Res. 2022 Dec;66(24):e2200104. doi: 10.1002/mnfr.202200104. Epub 2022 Oct 27. PMID: 36213967; PMCID: PMC10078384. https://pubmed.ncbi.nlm.nih.gov/36213967/